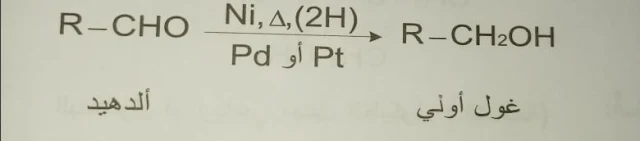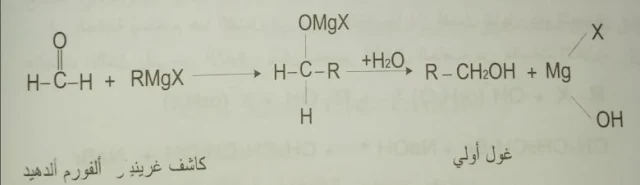- الطرائق العامة لتحضير الكحولات
- الطرائق الخاصة لتحضير الكحولات
- الميثانول CH3OH أو كحول الخشب
- الايثانول (كحول الحبوب) C2H5OH
تحضير الكحولات (Preparation of alcohols)
تحضر الكحولات وفق طرائق عامة وطرائق خاصة لنتحدث أولاً عن الطرائق العامة
الطرائق العامة لتحضير الكحولات
1- من الالكنات alkanes :
هناك بعض الطرق والتي يمكن اتباعها لتحضير بعض الكحولات مثل إضافة ثنائي البوران diborane إلى الألكنات وكذلك اكسدتها بواسطة البرمنغنات او بواسطة إضافة مركبات الزئبق وانتزاعها أو ضم الماء إليها
2- حلمهة هاليدات الالكيل :
Hydrolysis of alkyl halides
في الحقيقة يستخدم هذا التفاعل في حالات قليلة جداً لأن أفضل تفاعل عام لتحضير هاليدات الالكيل يأتي من الكحولات ، يمكن تحضير الكحولات الخاصة من هاليدات الالكيل
3- إرجاع المركبات الكربونيلية :
يمكن إرجاع مجموعة الكربونيل بوجود حفاز معدني مثل Ni أو Pt أو Pd أو (LiAlH4 أو NaBH4) حيث يتم إرجاع المركبات الكربونيلية إلى ما يلي :
- إرجاع الالدهيدات ويعطي الكحولات الأولية
- إرجاع الكيتونات ويعطي الاغوال الثانوية
- إرجاع الاسترات والحموض الكربوكسيلية
4- ضم كواشف غرينيار RMgX إلى المركبات الكربونيلية :
- عند ضم كواشف غرينيار إلى الالدهيدات نحصل على الكحولات الثانوية عدا مع الفورم الدهيد أو الدهيد النمل H-CHO فالناتج حتماً كحول أولي
- وتتشكل الكحولات الثانوية من بقية الالدهيدات.
- أما تفاعل الكيتونات مع كواشف غرينيار فتعطي الكحولات الثالثية.
- كما أن ضم كواشف غرينيار إلى الاسترات يعطي كحول أولي وكيتون يتفاعل مع كاشف غرينيار ونحصل على كحول ثالثي .
- بتالي فإن الناتج النهائي للتفاعل الاسترات مع كواشف غرينيار هو كحول أولي وكحول ثالثي.
- أما ضم الحموض الكربوكسيلية إلى كواشف غرينيار فلا يعطي الكحولات وإنما يؤدي إلى تشكل الفحوم الهيدروجينية.
نلاحظ أنه بضم كواشف غرينيار إلى المركبات الكربونيلية عدا الحموض الكربوكسيلية تمكننا من الحصول على كحولات أكثر تعقيداً من ناحية السلسلة الكربونيلية وبشكل سريع.
الطرائق الخاصة لتحضير الكحولات
1- تخمر النباتات الحاوية على النشاء للحصول على الايتانول ethanol :
يتم تحضير الاغوال بالحلمهة الحمضية للنشاء الذي يتحول إلى سكر ثنائي هو المالتوز maltose يتفكك لاحقاً إلى الغلوكوز glucose الذي يعطي بالتخمر الأنزيمي الغول الايتيلي ethanol بنسبة 95%
2- تفاعل الهيدروجين مع أحادي أكسيد الكربون للحصول على الميتانول methanol :
يتم ذلك باستعمال مزيج من CO و H2 وبدرجة حرارة عالية جداً 350 C° وبوجود الكوبالت cobalt واكسيد الزنك zinc oxide وذلك وفق التفاعل التالي
مصدر الاغوال(الكحولات) واستخدامها :
<><>
مصدر الاغوال(الكحولات) واستخدامها :
1- الميثانول CH3OH أو كحول الخشب
- يوجد ضمن المواد الناتجة عن التقطير الإتلافي للخشب وهو شفاف ينحل في الماء بشتى النسب.
- يؤثر هذا الكحول في الجملة العصبية المركزية ويؤدي إلى تلف الأعصاب وأورام المخ وتقرحات في عصب الرؤية إذا تستخدم بتراكيز منخفضة أما التراكيز العالية فتسبب الموت والميثانول يتحول أنزيمياً وفق التفاعل التالي :
يستخدم الميثانول في :
- صناعة الفورم الدهيد formaldehyde
- مضاد تجمد
- محلات الورنيش
- وقود للطائرات
يتم تحضير الميثانول من :
- من التقطير الإتلافي للخشب
- من تفاعل الهيدروجين مع CO أحادي اكسيد الكربون وبدرجة حرارة عالية 350C° وبوجود الوسطاء الكوبالت وZnO
- أو Cr2O3 وفق التفاعل التالي :
2- الايثانول (كحول الحبوب) C2H5OH
- يعتبر الايثانول اقدم مركب كيميائي عضوي اصطناعي استخدمه الانسان.
- يستخدم الايثانول في الصناعة استخداماً واسعاً كمذيب لمواد الطلاء والورنيش والعطور والمنكهات، وكوسيط للتفاعلات الكيميائية، وفي عملية إعادة البلورة،
- أضف إلى ذلك أنه يُعد مادة أولية مهمة في اصطناع العديد من المواد مثل حمض الخل acetic acid وخلات الايتيل ethyl acetate والايثر ether العادي،
- كما يمكن استعماله كمصدر للطاقة الحرارية.
- يمتص الايثانول بشكل سريع في المعدة والأمعاء الدقيقة وعندما يصل تركيزه في الدم 1.5 ml/mg فإن مراكز التوازن العصبية لدى الإنسان تصاب بالخمول ويفقد السيطرة على إرادته.
- ويعد الايثانول المسؤول عن ظاهرة الإدمان الكحولي التي تخرب الكبد.
طرق تحضير الايثانول :
1- إماهة الايثلين الناتج عن تكسير البترول:
2- تخمير المواد السكرية والمركبات النشوية :
- إن الايثانول المسوق تجارياً باستثناء ما يستخدم في المشروبات الكحولية عبارة عن مزيج مؤلف من 95% كحول و 5% ماء
- يعرف الايثانول النقي بالكحول المطلق ويمكن الحصول عليه بمعالجة الغول بمعدن المغنيزيوم الذي يحول الماء إلى Mg(OH)2 غير الذواب ويقطر الكحول بعدئذٍ
وتستخدم الديولات البسيطة مثل ايثلين غليكول ethylene glycol وبروبلين غليكول propylene glycol في صناعة البوليميرات polymers. ويفيد الايثلين غليكول كذلك في منع التجمد فهو المكون الرئيسي في مانع التجمد antifreeze الذي يضاف لماء محرك السيارة.
- أما الغليسرين أو الغليسرول فيوجد في الزيوت والدهون متحداً مع الحموض العضوية، يستخلص كناتج ثانوي أثناء صناعة الشحوم والشموع وفي صناعة الصابون.
- والغليسرول هو عبارة عن سائل لزج طعمه حلو، عديم اللون يمتزج بالماء بشتى النسب،
- يستعمل كعامل مرطب في صناعة التبغ وفي صناعة المستحضرات المطرية للجلد وفي صناعة اللدائن والسلوفان، ومن أهم مشتقاته ثلاثي نترو الغليسرين (trinitroglycerin TNG) .